慢性肾脏病(CKD)已成为一项全世界公共的健康问题,患病率和医疗花销不断走高,给个人和政府都造成了沉重的经济负担。终末期肾病(ESRD)患者是肾功能逐渐丧失的晚期患者,其并发症和死亡风险非常高,而且预期寿命也明显短于普通人群。通常,免疫异常被认为是并发症的催化因素,也是导致ESRD死亡的主要危险因素之一。在过去的几十年中,ESRD相关的免疫异常研究已经取得了巨大的进步,然而,导致这些异常变化的潜在分子机制仍然未知。因此,目前临床上还缺乏对于这些患者免疫系统方面的有效干预措施。转录组分析可以识别潜在的致病驱动因素和生物学靶标。前期对ESRD的转录谱研究主要集中在对大细胞群体中基因平均表达水平。单细胞转录组测序技术(scRNA-seq)使得我们可以在单个细胞水平上表征单个细胞中的基因表达谱,并建立单细胞水平的基因调控网络。暨南大学附属第一医院和南方科技大学第一附属医院联合开展了关于终末期肾病(ESRD)的单细胞测序分析研究,相关结果发表在Nephrol Dial Transplant上。
 文章题目:A single-cell map for the transcriptomic signatures of peripheral blood mononuclear cells in end-stage renal disease
文章题目:A single-cell map for the transcriptomic signatures of peripheral blood mononuclear cells in end-stage renal disease 中文:终末期肾病(ESRD)中PBMCs的单细胞转录图谱分析
中文:终末期肾病(ESRD)中PBMCs的单细胞转录图谱分析 发表杂志:Nephrol Dial Transplant
发表杂志:Nephrol Dial Transplant 影响因子:4.531
影响因子:4.531 发表年份:2019年
发表年份:2019年 样本类型:20个志愿者的外周血单核细胞(10个健康志愿者;10个终末期肾病患者);
样本类型:20个志愿者的外周血单核细胞(10个健康志愿者;10个终末期肾病患者); 样本处理:用EDTA抗凝外周血,Ficoll-Hypaque密度梯度离心分离PBMCs,每组10个样本混池为1份样本,采用10XGenomics进行单细胞转录组测序;
样本处理:用EDTA抗凝外周血,Ficoll-Hypaque密度梯度离心分离PBMCs,每组10个样本混池为1份样本,采用10XGenomics进行单细胞转录组测序; 获得数据:健康对照组测得12981个细胞,ESRD组测得9578个细胞;
获得数据:健康对照组测得12981个细胞,ESRD组测得9578个细胞; 数据分析:①细胞聚类和注释;②细胞特异性基因的筛选与鉴定;③ ESRD相关特征途径分析;④调节子活性分析。
数据分析:①细胞聚类和注释;②细胞特异性基因的筛选与鉴定;③ ESRD相关特征途径分析;④调节子活性分析。 文献特色:研究领域热;应用新技术(scRNA-seq);根据细胞类型(单核细胞、NK细胞、B细胞、T细胞)进行个性化分析。不足之处:样本混池测序分析限制了后续样本数的增加和结果的推广。
文献特色:研究领域热;应用新技术(scRNA-seq);根据细胞类型(单核细胞、NK细胞、B细胞、T细胞)进行个性化分析。不足之处:样本混池测序分析限制了后续样本数的增加和结果的推广。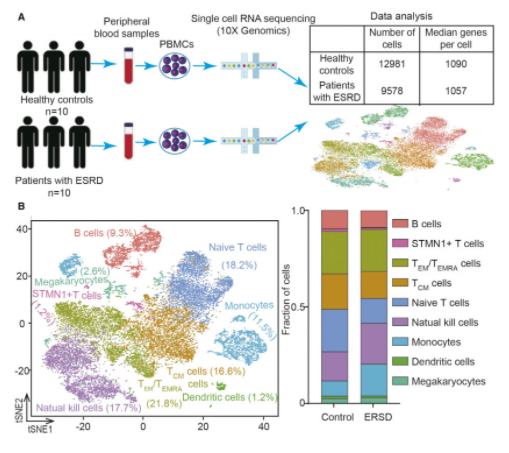
外周血PBMCs分离流程及单细胞转录组的无监督聚类分析
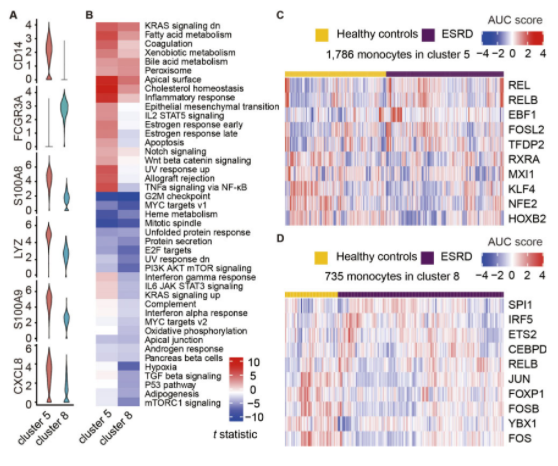
单核细胞的单细胞分析
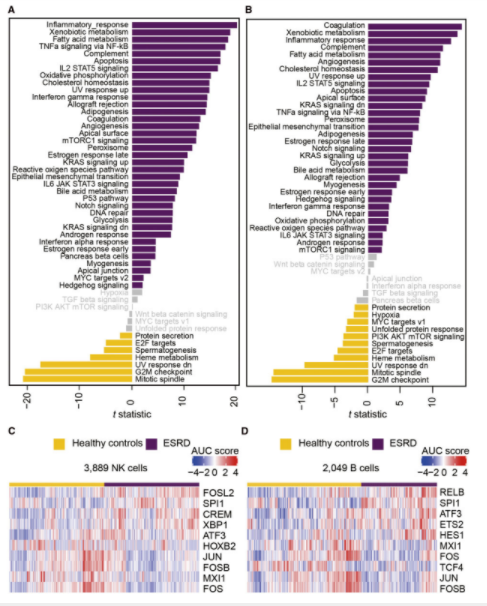
NK和B细胞中与ESRD相关的分子信号途径和转录因子
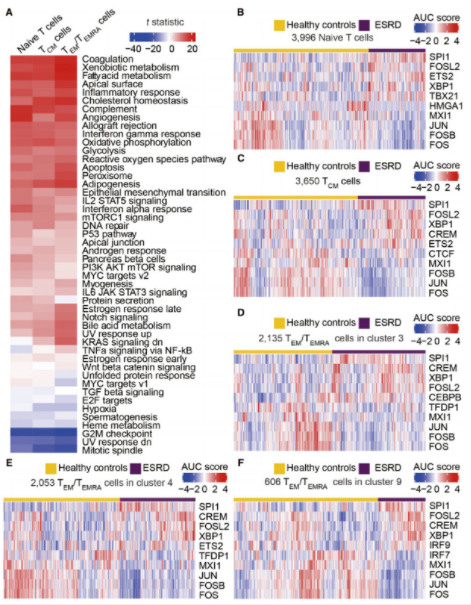
T细胞中与ESRD相关的分子信号途径和转录因子
本项研究中,研究人员募集了20个志愿者(10个健康志愿者;10个ESRD志愿者),采集外周血,分离单核细胞(PBMCs),并将每组样本进行混池后进行单细胞转录组测序。健康对照组和ESRD组分别测得12981和9578个细胞的转录组数据。随后,进行了无监督聚类分析进行细胞聚类和注释,并在主要的细胞类型(单核细胞、NK细胞、B细胞、T细胞)中筛选关键的分子信号通路和调节子活性分析。最终,研究人员确定了14个白细胞簇,对应于6种已知的PBMC细胞类型。对来自ESRD患者和健康志愿者的细胞数据进行比较揭示了生物学过程的多种变化。研究人员还注意到,在ESRD中,与ESRD相关的炎症反应增加、补体级联和细胞代谢增强,以及与细胞周期进程相关的活性大大降低。此外,还确定了细胞类型特异性的驱动ESRD相关转录组变化的候选转录因子的众多个基因。以上结果揭示了细胞类型特异性的ESRD相关分子信号途径和转录因子。值得注意的是,混池测序分析限制了后续样本的增加和结果的推广。后续,更多的单细胞数据集可以补充当前的图谱,并推动操控ESRD免疫细胞功能新疗法的发展。